18 septembre 2024
 3 min
3 min

Bienvenue sur LeFil.vet
L'accès au site web nécessite d'être identifié.
Merci de saisir vos identifiants de connexion.
Indiquez votre email dans le champ ci-dessous.
Vous recevrez un email avec vos identifiants de connexion.


En prévoyant une exception à l'interdiction de l'usage vétérinaire du remdésivir, ou de son métabolite actif le GS 441524, la réglementation européenne n'interdit pas aux praticiens de prescrire cet antiviral, mais seulement chez le chat et en traitement de la péritonite infectieuse féline.
Cette exception découle d'un règlement d'exécution européen, sur l'application de l'article 107(6) du règlement « médicament vétérinaire » (règlement 2019/6) qui porte sur le recours à des antimicrobiens « hors AMM », dans le cadre de la cascade. Publié le 19 juillet dernier, ce règlement d'application s'appuie sur un avis scientifique de l'Agence européenne du médicament (EMA), publié en juin 2023.
Ces dispositions s'inscrivent en complément des restrictions préexistantes, liées au dispositif de la cascade, aux LMR (limites maximales de résidus), à la loi de santé animale, au droit national (relatifs aux antibiotiques critiques ou aux médicaments hospitaliers en France).
Ce règlement d'exécution liste 12 antimicrobiens (ou familles d'antimicrobiens) pour lesquels les dispositions de la cascade seront restreintes. L'objectif poursuivi relève surtout du domaine de la santé publique : préserver l'efficacité de médicaments critiques pour l'homme.
Ainsi, sans surprise, 9 des 12 anti-infectieux concernés sont des antibiotiques. Et 6 parmi eux ont des AMM vétérinaires :
Les 3 autres sont des antibiotiques à usage humain : les rifamycines (hors rifaximine), les riminoférazines et antituberculeux, la mupirocine. En pratique, ils ne disposent pas de LMR, donc ne peuvent pas être utilisés chez les animaux de production, et hormis la mupirocine, sont interdits de tout usage vétérinaire en France (y compris chez les animaux de compagnie).
La prescription « hors AMM » des antibiotiques visés par le nouveau règlement reste possible, mais soumise au préalable à une analyse bactériologique identifiant le ou les pathogènes en cause, et à un antibiogramme dont les résultats permettront – de manière obligatoire et contraignante – d'attester le besoin de recourir à ces molécules, en l'absence de sensibilité à des molécules moins risquées selon la classification actuelle.
Les antibiotiques sont effectivement classés en 4 catégories selon le risque croissant qu'ils représentent (vis-à-vis de l'émergence de résistance) : de D (première intention) à A (à éviter). Et dans sa prescription « hors AMM », le vétérinaire devrait respecter aussi cette hiérarchie, en choisissant par exemple un antibiotique de première plutôt que de deuxième intention, à l'instar de l'amoxicilline seule (si le germe y est sensible) plutôt qu'une association amoxicilline-acide clavulanique.
En France, depuis maintenant 8 ans, un antibiogramme est déjà obligatoire avant de prescrire (hors AMM ou non) les antibiotiques « critiques » que sont les fluoroquinolones et les céphalosporines de dernières générations. Les nouvelles restrictions rendent le résultat contraignant et l'élargissent aux 7 autres familles ou molécules.
Les antibiotiques de première intention (benzylpénicilline ou amoxicilline seule par exemple) – catégorie D selon la classification européenne – ne sont pas visés par ces restrictions. De même que certains antibiotiques de seconde intention – catégorie C –, comme les macrolides et apparentés ou les céphalosporines de première et seconde générations.
La réglementation n'est pas complètement déconnectée de la pratique. Ainsi, des dérogations sont-elles prévues à l'évaluation de la sensibilité des antibiotiques :
Inversement, des restrictions supplémentaires s'appliquent à quelques cas particuliers. Ainsi :
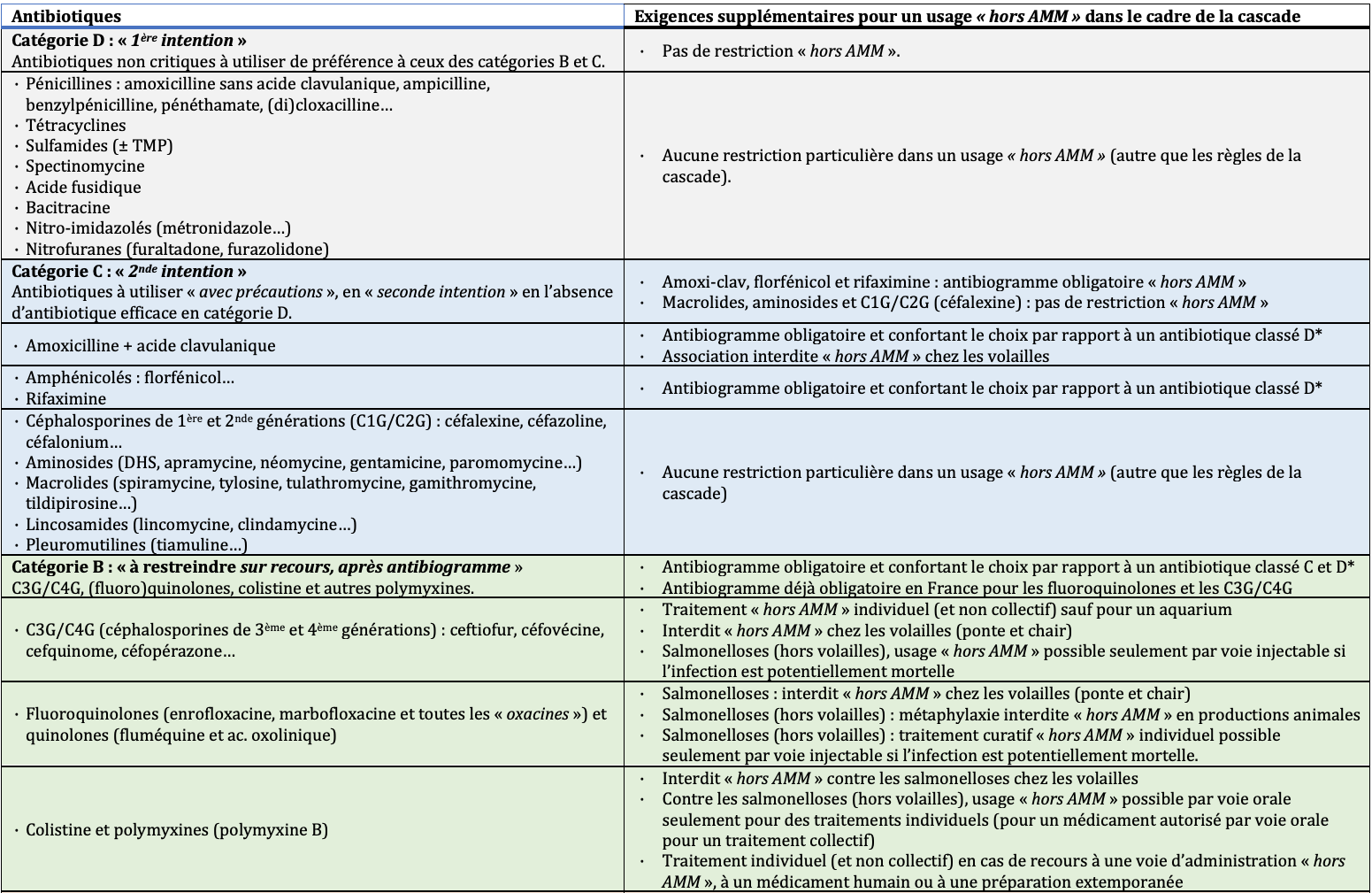
Le tableau en bas de ce Fil récapitule l'ensemble de ces restrictions.
Le remdésivir est un antiviral, dont l'usage hors AMM est interdit par ce règlement. À une exception près : le traitement de la PIF. Cette exception figure dans le rapport scientifique de l'EMA, publié en juin 2023. Les experts se sont appuyés sur des données d'efficacité de la molécule contre cette maladie (pour laquelle aucun traitement n'est disponible), et un usage restreint aux chats, ce qui limite le risque d'émergence de résistance. La commission européenne a suivi cet avis. L'un des critères pris en compte pour déterminer les restrictions d'usage hors AMM est en effet l'effet négatif que peuvent avoir ces restrictions, par exemple une maladie qui ne peut plus être traitée.
En pratique, il n'est donc pas interdit aux vétérinaires de prescrire hors AMM cet antiviral, pour traiter un chat atteint de PIF.
Toutefois, le médicament humain commercialisé en France (sous la marque Veklury°, indiqué en traitement de la Covid) est réservé à l'usage hospitalier, donc inaccessible aux vétérinaires (y compris par importation depuis un pays d'Europe).
Plusieurs pharmacies spécialisées proposent en revanche des préparations magistrales (de GS 441524, le métabolite actif du remdésivir), pour administration orale aux chats. Ces préparations extemporanées peuvent donc être prescrites et délivrées.
Autre molécule listée par le nouveau règlement : l'amphotéricine B peut être prescrite hors AMM, de manière restreinte pour le traitement d'un cas de leishmaniose canine, en dernier recours. En pratique toutefois, la forme orale à usage humain n'est pas efficace contre la maladie (la molécule n'est pas aborbée par voie digestive), et la forme injectable fait partie de la réserve hospitalière en France, et n'est donc pas accessible aux vétérinaires.
Enfin, les échinocandines (caspofungine, micafungine, anidulafungine, rézafungine) sont également utilisables hors AMM, mais uniquement pour le traitement de dernier recours d'un cas d'infection fongique (candidose ou aspergillose invasive), et sur la base d'un test de sensibilité. En pratique toutefois encore, les médicaments humains commercialisés en France (poudre pour solution injectable intraveineuse) font partie de la réserve hospitalière, et sont inaccessibles aux vétérinaires.
Les équidés sont exclus de ces nouvelles restrictions réglementaires. En effet, des dispositions particulières les concernent, et la liste des substances essentielles aux équidés est en cours de révision.
Un texte spécifique est également en cours pour l'application de la cascade en aquaculture. Les poissons, coquillages et autres animaux aquatiques producteurs de denrées alimentaires, ne sont donc pas concernés non plus. Les poissons d'ornement, en revanche, sont inclus.
Toutes les autres espèces animales sont concernées, de production comme de compagnie. Un délai d'adaptation de 2 ans est néanmoins concédé avant l'application du nouveau règlement, dont les mesures entreront donc en vigueur le 8 août 2026.
Tableau récapitulatif des nouvelles restrictions
18 septembre 2024
 3 min
3 min

17 septembre 2024
 7 min
7 min

16 septembre 2024
 5 min
5 min

12 septembre 2024
 5 min
5 min

11 septembre 2024
 8 min
8 min





